Con il presente articolo si vuole fornire una sintesi aggiornata dei principali meccanismi molecolari che regolano l’ipertrofia del muscolo scheletrico umano indotta dall’allenamento contro resistenza.
Sintesi
Il muscolo scheletrico svolge un ruolo fondamentale nella funzione fisica e nella salute metabolica. È un tessuto altamente adattabile che risponde all’esercizio contro resistenza (RE; carico) andando incontro a ipertrofia oppure, in condizioni di disuso muscolare, l’esercizio contro resistenza attenua la perdita di massa muscolare.
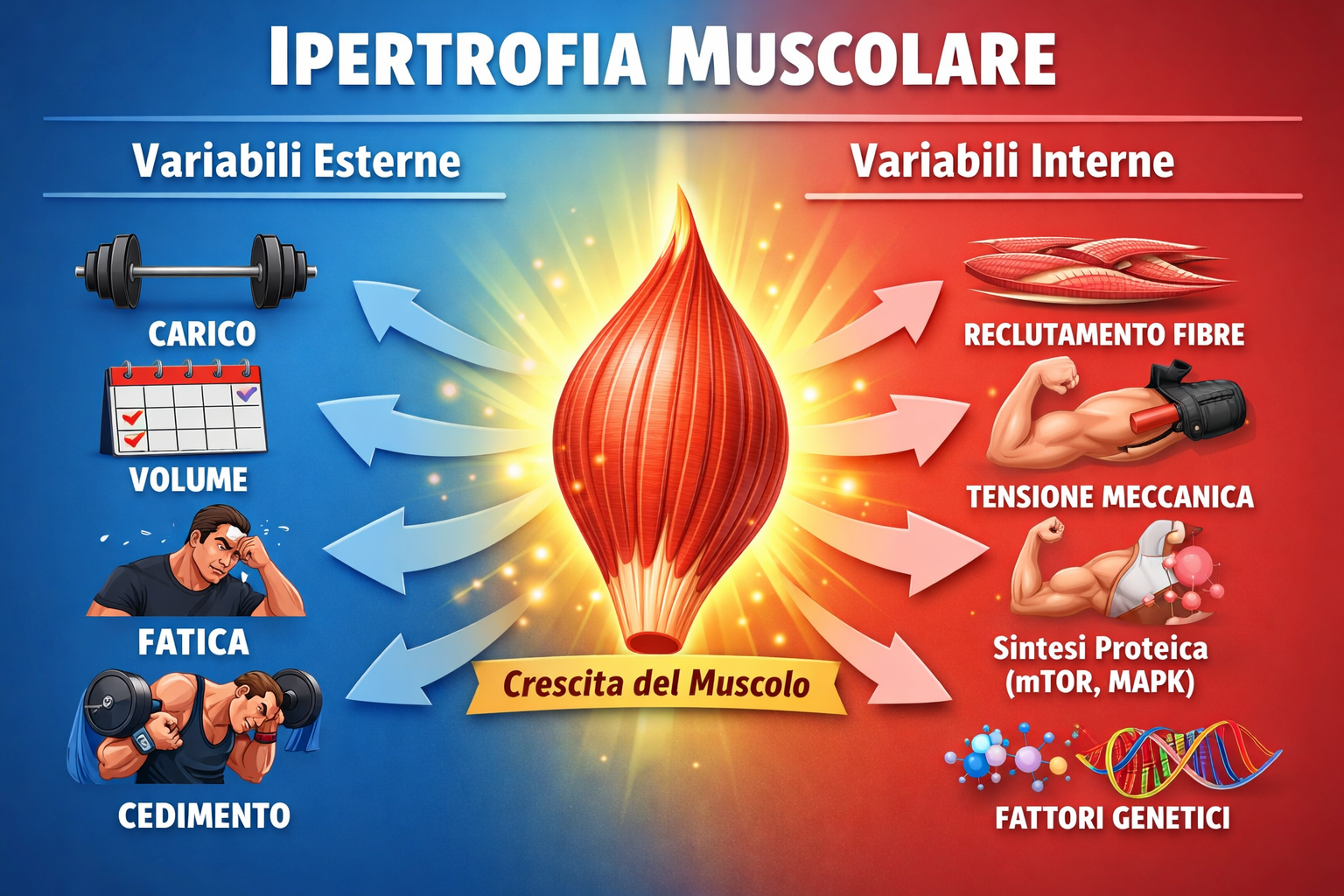
L’ipertrofia del muscolo scheletrico indotta dall’allenamento contro resistenza (RET) è il risultato dell’interazione tra variabili esterne (ad esempio programmazione dell’esercizio, dieta, alcuni integratori) e variabili interne (ad esempio meccanotrasduzione, ribosomi, espressione genica, attività delle cellule satelliti).
L’esercizio contro resistenza rappresenta senza dubbio la più potente variabile esterna non farmacologica in grado di stimolare l’attivazione o la soppressione delle variabili interne associate all’ipertrofia muscolare o al contrasto della perdita muscolare da disuso.
In questo lavoro proponiamo che, nonostante l’ampia mole di ricerche sull’impatto delle variabili esterne sull’allenamento contro resistenza e sull’ipertrofia, le variabili interne (cioè la biologia intrinseca del muscolo scheletrico) siano predominanti nel regolare l’entità dell’ipertrofia in risposta agli stimoli esterni.
Pertanto, identificare le principali variabili interne derivate dal muscolo scheletrico che mediano la traduzione delle variabili esterne dell’esercizio contro resistenza sarà fondamentale per determinare le strategie più efficaci per promuovere l’ipertrofia muscolare in soggetti sani. Queste conoscenze contribuiranno anche a migliorare la funzione nei pazienti clinici, a rallentare il declino funzionale e a promuovere la mobilità fisica.
In questa revisione forniamo una prospettiva aggiornata, basata sulle evidenze, dei meccanismi che regolano l’ipertrofia del muscolo scheletrico indotta dall’allenamento contro resistenza.
Introduzione
Il muscolo scheletrico svolge un ruolo critico nella funzione fisica, nella performance atletica e nella salute metabolica, e una bassa massa muscolare è associata a una maggiore mortalità sia negli adulti sani sia negli adulti con comorbidità.
La regolazione della massa muscolare scheletrica è influenzata da diverse variabili che possono essere ampiamente classificate come variabili esterne o variabili interne. L’allenamento contro resistenza (RET) rappresenta il mezzo non farmacologico più potente per aumentare la massa muscolare scheletrica ed è una variabile esterna del sistema.
Al contrario, le variabili interne sono processi biologici sistemici o, più spesso, locali (all’interno del muscolo) che sostengono meccanisticamente l’ipertrofia in risposta a stimoli esterni come il RET (Figura 1).
Una questione cruciale è fino a che punto la manipolazione delle variabili esterne influenzi la risposta delle variabili interne nel determinare l’esito finale, cioè l’ipertrofia. A nostro avviso, identificare i principali bersagli molecolari del muscolo scheletrico attivati dall’esercizio contro resistenza che, con la ripetizione, sostengono l’ipertrofia muscolare indotta dal RET è fondamentale.
A livello molecolare, l’ipertrofia del muscolo scheletrico indotta dal RET (definita qui come un aumento dell’area di sezione trasversa assiale del muscolo o della fibra muscolare) negli adulti avviene a causa dell’accumulo di proteine cellulari (ad esempio miofibrillari, sarcoplasmatiche, mitocondriali) all’interno delle fibre muscolari preesistenti.
Sorprendentemente, rimaniamo in gran parte ignari delle precise adattamenti strutturali associati all’ipertrofia muscolare indotta dal RET. Tuttavia, è un assioma che l’ipertrofia richieda, tra gli altri processi, un’accumulazione netta di proteine muscolari, che si verifica quando il tasso di sintesi proteica muscolare (MPS) supera quello della degradazione proteica muscolare (MPB), la cui differenza algebrica è comunemente definita come bilancio proteico netto.
Al contrario, periodi prolungati di bilancio proteico netto negativo (MPB > MPS) si manifestano come atrofia muscolare scheletrica, che si verifica in vari scenari sistemici, come la riduzione dell’attività fisica e il riposo a letto, o locali, come l’immobilizzazione di un arto.
È importante sottolineare che molte malattie croniche, tra cui cancro, broncopneumopatia cronica ostruttiva (BPCO), malattie cardiovascolari, sepsi, uremia e ustioni, presentano componenti di perdita muscolare. Pertanto, identificare i meccanismi che regolano il turnover proteico muscolare a favore dell’anabolismo netto è una missione clinicamente rilevante tanto quanto lo è per gli atleti, se non di più.
Il controllo molecolare della MPS e della MPB è complesso e numerose cascate di segnalazione proteica determinano il bilancio proteico netto. Tuttavia, stiamo ancora decifrando quali segnali inneschino l’aumento della MPS e possano quindi contribuire all’ipertrofia del muscolo scheletrico.
MECCANOTRASDUZIONE
Come stimolo esterno, l’esercizio contro resistenza determina un carico meccanico sul muscolo scheletrico; tuttavia, i meccanismi attraverso i quali il muscolo scheletrico “percepisce” questo stimolo e avvia risposte che culminano nell’ipertrofia sono ancora in fase di chiarimento.
Sono stati identificati diversi complessi proteici come potenziali meccanosensori che agiscono da trasduttori molecolari durante la contrazione delle miofibre. La matrice extracellulare sembra svolgere un ruolo critico nella conversione dei segnali meccanici in segnali biochimici che, in ultima analisi, regolano il controllo della massa muscolare scheletrica.
I costameri collegano la matrice extracellulare al sarcolemma della miofibra, sono localizzati a livello del disco Z e agiscono trasmettendo la forza dal sarcomero alla matrice extracellulare. In presenza di stimoli meccanici, la fosfolipasi Cγ1 si colocalizza attorno alla chinasi di adesione focale (FAK), una proteina densamente localizzata nel costamero, e catalizza la conversione del fosfatidilinositolo 4,5-bifosfato in acido fosfatidico (PA).
L’acido fosfatidico sintetizzato attiva gli effettori della via HIPPO, Yes-associated protein 1 (YAP) e transcriptional coactivator with PDZ-binding motif (TAZ), attraverso una cascata di segnalazione. YAP e TAZ non solo controllano la crescita cellulare in Drosophila melanogaster e in alcuni tessuti dei mammiferi, ma regolano anche la proliferazione e la differenziazione dei mioblasti.
Sebbene non sia stato chiarito un collegamento meccanicistico diretto tra YAP e la segnalazione del complesso 1 del bersaglio meccanicistico della rapamicina (mTORC1), studi su modelli animali hanno dimostrato che l’aumento dell’espressione di YAP è sufficiente ad aumentare la massa muscolare scheletrica anche durante l’inibizione di mTORC1 tramite rapamicina.
YAP e TAZ possono inoltre svolgere un ruolo nella segnalazione anabolica indotta meccanicamente attraverso l’aumento dell’espressione dei geni Slc7a5 e Slc3a2, che codificano per trasportatori dell’amminoacido leucina, potenzialmente rendendo il muscolo caricato meccanicamente più sensibile alla sintesi proteica stimolata dalla leucina.
Inoltre, l’acido fosfatidico può modulare indirettamente l’ipertrofia muscolare scheletrica tramite la via HIPPO e attivare mTORC1. È stato dimostrato che l’esercizio contro resistenza è sufficiente ad aumentare la concentrazione locale di acido fosfatidico e che l’inibizione della sua produzione elimina i marcatori di attività di mTORC1 dopo sovraccarico meccanico del muscolo scheletrico.
Nel complesso, i sensori proteici basati sui costameri sembrano essere necessari per la segnalazione ipertrofica nel periodo immediatamente successivo all’esercizio.
VIA DI SEGNALAZIONE mTOR
Il complesso mTOR comprende una chinasi serina/treonina che nei mammiferi forma due complessi proteici distinti: mTORC1 e mTORC2. Entrambi contengono le subunità DEPTOR e mLST8, ma differiscono per sensibilità alla rapamicina, funzioni biologiche e subunità aggiuntive.
In termini generali, mTORC1 è considerato un regolatore della dimensione cellulare sensibile alla rapamicina ed è costituito, tra le altre, dalle subunità Raptor e PRAS40. Stimoli a monte come nutrienti (in particolare la leucina), fattori di crescita (ad esempio IGF-1) e stimoli meccanici (esercizio contro resistenza) vengono convertiti in segnali intracellulari che vengono rilevati dalle subunità di mTORC1.
Al contrario, mTORC2 è un regolatore insensibile alla rapamicina, coinvolto principalmente nel controllo della struttura del citoscheletro e della sopravvivenza cellulare, ed è composto da Rictor, mSIN1 e PROTOR 1/2.
L’aumento della sintesi proteica muscolare indotto da mTORC1 è stato a lungo un punto focale nello studio dell’ipertrofia muscolare. Due bersagli a valle frequentemente analizzati sono la p70S6 chinasi 1 (S6K1) e la proteina legante il fattore di inizio della traduzione 4E (4EBP-1). L’ipertrofia muscolare è stata correlata alla sintesi proteica basale e alla fosforilazione di S6K1 e 4EBP-1 indotta dall’esercizio contro resistenza.
Tuttavia, l’attivazione di mTORC1 contribuisce sì all’aumento della sintesi proteica, ma le risposte acute a breve termine (nelle ore successive all’esercizio) non sono sempre correlate all’ipertrofia cronica indotta dall’allenamento. Studi longitudinali mostrano che la sintesi proteica dopo una singola seduta diventa predittiva dell’ipertrofia solo dopo l’attenuazione del danno muscolare iniziale.
Nel complesso, mTORC1 svolge un ruolo importante nell’ipertrofia, ma i meccanismi sottostanti vanno oltre la semplice attivazione di questa via.
La traslocazione di mTORC1 verso il lisosoma è cruciale per la sua attivazione. L’esercizio contro resistenza induce la traslocazione di mTORC1 al lisosoma, e successivamente il complesso mTORC1-lisosoma si sposta verso la membrana cellulare, spesso in prossimità dei capillari. Questa localizzazione periferica potrebbe favorire la sintesi proteica grazie alla maggiore vicinanza a nutrienti, fattori di attivazione e apparato di traduzione.
Oltre ai meccanismi sensibili alla rapamicina, esistono componenti di segnalazione mTOR-indipendenti che contribuiscono alla sintesi proteica e all’ipertrofia. Studi su modelli animali e umani mostrano che l’inibizione di mTORC1 non abolisce completamente l’aumento della massa muscolare indotto dall’allenamento. In questo contesto, vie come MAPK-ERK1/2 possono agire in parallelo o in sinergia con mTORC1 per stimolare la traduzione proteica.
In sintesi, le vie di segnalazione correlate a mTOR sono centrali per l’anabolismo muscolare, ma i contributi specifici di mTORC1 e mTORC2 e delle vie parallele sono ancora oggetto di definizione.
BIOGENESI RIBOSOMIALE
Il ribosoma è una macchina molecolare composta da RNA ribosomiale (rRNA) e proteine, essenziale per la traduzione delle proteine. Un ribosoma funzionalmente attivo (80S) è formato da due subunità (60S e 40S) ed è il risultato dell’assemblaggio coordinato di oltre 80 proteine e quattro rRNA.
La biogenesi ribosomiale è un processo ad alto costo energetico ed è l’unico che richiede l’attivazione coordinata di tutte e tre le RNA polimerasi. L’aumento della sintesi proteica indotto dall’esercizio può avvenire attraverso:
- maggiore efficienza traduttiva (più traduzione con lo stesso numero di ribosomi);
- maggiore capacità traduttiva (aumento del numero di ribosomi disponibili).
La biogenesi ribosomiale è emersa come un potenziale regolatore dell’ipertrofia indotta dall’allenamento contro resistenza. Nei modelli animali di sovraccarico estremo, l’aumento del contenuto totale di RNA (indicatore indiretto di ribosomi) è fortemente associato all’ipertrofia. Tuttavia, tali modelli producono livelli di crescita muscolare molto superiori a quelli osservati nell’uomo.
Negli esseri umani allenati, una singola seduta di esercizio contro resistenza aumenta la sintesi proteica senza un parallelo incremento misurabile dell’RNA totale. I marcatori di espressione genica ribosomiale tendono a stabilizzarsi dopo poche settimane di allenamento e, in alcuni casi, ritornano ai livelli basali nel lungo periodo.
Questo suggerisce che l’aumento iniziale della capacità traduttiva sia rapido e poco specifico, mentre con il progredire dell’allenamento la risposta diventa più efficiente e specifica per lo stimolo, riducendo la necessità di ulteriore aumento del numero di ribosomi.
Esiste inoltre una notevole eterogeneità individuale: soggetti con grandi aumenti di massa muscolare possono mostrare regolazioni ribosomiali simili a soggetti che non rispondono all’allenamento. Attualmente, le evidenze sul ruolo determinante della biogenesi ribosomiale nelle differenze individuali di ipertrofia sono suggestive ma non conclusive.
ESPRESSIONE GENICA
Le tecnologie “omics” hanno dimostrato che l’esercizio modifica l’espressione di migliaia di geni nel muscolo scheletrico. Tuttavia, l’interpretazione funzionale di questi cambiamenti è complessa: non tutte le variazioni trascrizionali si traducono in cambiamenti proteici o in ipertrofia.
Analisi su grandi coorti mostrano che l’allenamento contro resistenza regola prevalentemente geni coinvolti nel rimodellamento della matrice extracellulare. Tuttavia, molti di questi cambiamenti non sono direttamente associati all’aumento della massa muscolare.
Gli autori propongono che l’analisi delle risposte individuali, anziché la media di gruppo, sia più efficace per identificare le firme trascrizionali specifiche dell’ipertrofia. Studi recenti hanno identificato un set di geni la cui regolazione è fortemente correlata alla crescita muscolare cronica, in particolare attraverso modifiche delle regioni non tradotte (UTR) dell’mRNA, senza variazioni nei livelli totali di mRNA.
Questi risultati suggeriscono che la regolazione post-trascrizionale giochi un ruolo cruciale nell’ipertrofia e potrebbe spiegare la frequente discordanza tra livelli di mRNA e proteine.
ORMONI ANABOLICI SISTEMICI INDOTTI DALL’ESERCIZIO
Ormoni tradizionalmente considerati anabolici (testosterone, GH, IGF-1) aumentano transitoriamente dopo una seduta di esercizio contro resistenza. Tuttavia, non vi sono prove che questi aumenti acuti siano causalmente responsabili dell’ipertrofia muscolare.
Numerosi studi mostrano che:
- l’aumento acuto di GH o IGF-1 non è correlato alla sintesi proteica né all’ipertrofia;
- la somministrazione esogena di GH o IGF-1 non migliora la crescita muscolare in soggetti sani o anziani;
- l’aumento endogeno di testosterone dopo l’esercizio è troppo breve e quantitativamente irrilevante rispetto alla variazione fisiologica giornaliera.
Al contrario, la densità del recettore androgeno (AR) nel muscolo risulta più predittiva della risposta ipertrofica rispetto alle variazioni ormonali sistemiche. Inoltre, le donne, pur avendo concentrazioni di testosterone molto inferiori, mostrano guadagni relativi di forza e ipertrofia simili agli uomini.
DANNO MUSCOLARE INDOTTO DALL’ESERCIZIO
Il danno muscolare aumenta l’infiammazione e attiva le cellule satelliti, ma non è un prerequisito per l’ipertrofia. Le misure indirette di danno (dolore, creatinchinasi) sono poco affidabili e non correlate in modo consistente con la sintesi proteica o la crescita muscolare.
Nelle fasi iniziali dell’allenamento, l’aumento della sintesi proteica serve principalmente alla riparazione del danno. Solo dopo la sua attenuazione la sintesi proteica contribuisce in modo diretto all’ipertrofia. Inoltre, il muscolo può riparare danni locali anche indipendentemente dalle cellule satelliti, tramite meccanismi di migrazione nucleare.
METABOLITI
I metaboliti prodotti durante la contrazione (lattato, ioni idrogeno, fosfato inorganico) sono stati ipotizzati come segnali ipertrofici, ma non esistono evidenze causali solide che colleghino direttamente questi metaboliti all’ipertrofia muscolare nell’uomo.
Anche protocolli che aumentano fortemente l’accumulo metabolico (come l’allenamento con restrizione del flusso sanguigno) non producono ipertrofia superiore all’allenamento tradizionale. Inoltre, forme di esercizio che producono elevati metaboliti (endurance, sprint) non inducono ipertrofia comparabile al RET.
MALATTIA, INVECCHIAMENTO E IPERTROFIA MUSCOLARE
Nelle malattie croniche e nell’invecchiamento, la perdita muscolare è dovuta principalmente a un bilancio proteico negativo cronico, sostenuto da:
- aumento della proteolisi;
- riduzione della sintesi proteica;
- infiammazione sistemica;
- ridotta attività fisica.
L’allenamento contro resistenza può attenuare o prevenire la perdita muscolare in molte condizioni cliniche, anche se spesso si tratta di mitigazione dell’atrofia più che di vera ipertrofia.
Con l’invecchiamento si sviluppa una condizione di resistenza anabolica, in cui la risposta della sintesi proteica agli stimoli è attenuata. Nonostante ciò, il RET rimane lo stimolo più efficace per preservare forza, funzione e massa muscolare.
CONCLUSIONI E PROSPETTIVE FUTURE
L’ipertrofia del muscolo scheletrico è il risultato di una complessa interazione tra variabili esterne e interne. L’allenamento contro resistenza è il più potente stimolo esterno, ma sono le variabili interne a determinare l’entità dell’adattamento.
Meccanotrasduzione, regolazione trascrizionale e capacità/efficienza traduttiva emergono come meccanismi chiave. Sebbene mTOR sia centrale, non è l’unico regolatore dell’ipertrofia. Futuri studi, sfruttando tecnologie avanzate (single-cell, RNA-seq), saranno fondamentali per chiarire i determinanti molecolari della crescita muscolare nell’uomo.
Mariano Rubiu
Personal Trainer
Chinesiologo Dott. Scienze Motorie




















